Novo algoritmo identifica 35 novas espécies bacterianas a partir de isolados clínicos
Análise genômica de bactérias não cultivadas identificou 61 bactérias, destas, 35 eram até então desconhecidas. Os pesquisadores classificaram as restantes 26 espécies como difíceis de identificar
05/02/2024
O estudo foi conduzido entre dezembro de 2014 e janeiro de 2022 e utilizou informações clínicas, moleculares e fenotípicas sobre espécies bacterianas. Novo algoritmo demonstra ser uma ferramenta poderosa para detecção e identificação de novos organismos bacterianos
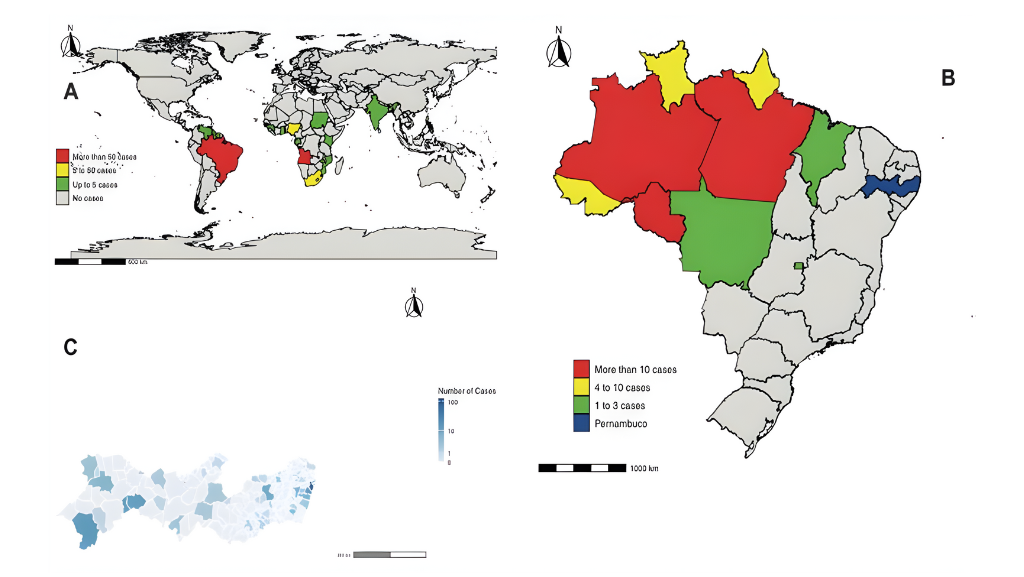
Em um estudo recente publicado na revista científica BMC Microbiology intitulado “Novel Organism Verification and Analysis (NOVA) study: identification of 35 clinical isolates representing potentially novel bacterial taxa using a pipeline based on whole genome sequencing”, os pesquisadores desenvolveram o algoritmo Novel Organism Verification and Analysis (NOVA) para analisar sistematicamente isolados bacterianos não identificados utilizando métodos tradicionais, como espectrometria de massa por dessorção a laser assistida por matriz com analisador por tempo de voo (MALDI-TOF MS) e sequenciamento parcial do gene do RNA ribossomal 16s (16S rRNA) usando sequenciamento do genoma completo (WGS). O estudo inovador liderado pelo Dr. Daniel Goldenberger, PhD, da Universidade de Basileia, Suíça, analisou 61 patógenos bacterianos desconhecidos, encontrados em amostras de sangue e tecidos de pacientes com diversas condições médicas.
Para o estudo, os pesquisadores do Hospital Universitário de Basileia, estudaram novos isolados bacterianos, incluindo aqueles clinicamente relevantes e aqueles cuja identificação foi problemática. Eles forneceram sequências genômicas de vários organismos bacterianos para aumentar os dados epidemiológicos e taxonômicos. A equipe também analisou dados clínicos sobre pacientes e a importância clínica dos isolados bacterianos para melhorar o conhecimento ecológico e clínico de novos organismos bacterianos.
Os resultados foram surpreendentes. Das 61 bactérias analisadas, 35 (57%) eram até então desconhecidas. As 26 (43%) restantes foram classificadas como difíceis de identificar. Os autores observaram que espécies de Corynebacterium sp. (n = 6) e Schaalia sp. (n = 5), ambos bacilos Gram-positivos, foram os gêneros predominantes. Vinte e sete das 35 cepas foram isoladas de amostras de tecidos profundos ou hemoculturas, sendo sete das 35 clinicamente relevantes. A equipe identificou quatro isolados como Gulosibacter hominis e um como Pseudoclavibacter triregionum. Além disso, identificaram duas cepas, cada uma dentro dos gêneros Clostridium, Anaerococcus, Peptoniphilus e Desulfovibrio. Os pesquisadores detectaram uma nova espécie para cada um dos seguintes gêneros Citrobacter, Dermabacter, Lancefieldella, Helcococcus, Neisseria, Paenibacillus, Ochrobactrum, Porphyromonas, Pantoea, Pseudomonas, Pseudoclavibacter, Pusillimoas, Psychrobacter, Sneathia, Tessaracoccus e Rothia.
Contrariando a ideia de um “alerta microbiológico”, o Dr. Goldenberger esclarece que se trata do resultado de oito anos de trabalho meticuloso na coleta dessas bactérias. “O foco principal é mostrar o potencial para detectar novas bactérias e o nosso novo algoritmo mostra como detectá-las”, aponta. O pesquisador também destacou que a identificação precisa de microrganismos torna-se fundamental para a prática clínica, proporcionando um reconhecimento eficiente e contribuindo para decisões embasadas no tratamento com antibióticos. “Com base em dados clínicos recentemente publicados, a interpretação dessas informações é facilitada, destacando a importância desse avanço na área da microbiologia”, acrescentou.
Questionado sobre o risco dessas bactérias e as implicações na saúde pública, o Dr. Goldenberger explicou que não se trata de organismos patogênicos, como é o caso do Streptococcus pyogenes. Segundo ele, essas bactérias fazem parte da microbiota humana da pele e das mucosas, incluindo a intestinal. “Por fazerem parte das bactérias benéficas à saúde, medidas normais de higiene são eficazes na prevenção e propagação, inclusive em ambientes hospitalares, assinalou o pesquisador.
O ambiente hospitalar possui uma microbiota composta por uma diversidade de microrganismos, tanto patogênicos quanto não patogênicos, aos quais pacientes, visitantes e profissionais de saúde estão expostos diariamente. O biomédico microbiologista Dr. Jailton Lobo, explica que muitos desses microrganismos, na maioria das vezes, apresentam baixo risco de infecção, uma vez que também compõem a microbiota humana normal. Exemplos incluem espécies dos gêneros Corynebacterium e Bacillus, espécies de Staphylococcus coagulase negativo. Ainda segundo ele, o ambiente das Unidades de Terapia Intensiva (UTIs) geralmente concentram uma maior prevalência de microrganismos patogênicos, inclusive aqueles que desenvolveram resistência aos antibióticos, como Staphylococcus aureus resistente à meticilina (MRSA), Enterococcus resistente à vancomicina (VRE), Enterobacterales resistentes aos carbapenêmicos (CRE), Acinetobacter baumannii resistente aos carbapenêmicos (CRAB) e Pseudomonas aeruginosa resistente aos carbapenêmicos (CRPA).
“Esses microrganismos compõem a lista de microrganismos prioritários da Organização Mundial de Saúde (OMS), devido ao seu elevado perfil de resistência aos antibióticos e para os quais torna-se fundamental o desenvolvimento de novos antibióticos”, assinala o Dr. Lobo ao reconhecer que estudos como este liderado pelo Dr. Goldenberger são fundamentais. “Ao realizar o mapeamento de microrganismos circulantes, proporcionam o conhecimento dos microrganismos presentes no ambiente, os riscos que representam à saúde e as medidas de prevenção que podem ser implementadas para evitar a propagação desses microrganismos”, enfatiza.
No Brasil, a maioria das análises sobre os microrganismos presentes no ambiente hospitalar é derivada de dados epidemiológicos elaborados pela equipe do laboratório de Microbiologia e pelos profissionais das Comissões de Controle de Infecção Hospitalar (CCIHs), obtidos a partir dos resultados de culturas microbiológicas e testes de sensibilidade aos microrganismos realizados nos laboratórios. “Entretanto, é importante ressaltar que alguns microrganismos não são facilmente cultiváveis e identificados pelas metodologias comumente utilizadas na maioria dos laboratórios de Microbiologia Clínica, o que requer a utilização de metodologias mais sensíveis, porém mais caras, como o sequenciamento do genoma completo, que foi essencial para a identificação de 35 novas espécies no estudo realizada pela equipe da Basileia”, conclui o Dr. Lobo.
No estudo liderado pelo Dr. Goldenberger, um dos patógenos difíceis de identificar pode ser clinicamente relevante. Ele foi encontrado no polegar inflamado de um paciente após uma mordida de cachorro. Um grupo de pesquisa canadense recentemente também isolou esta bactéria de feridas causadas por mordidas de cães ou gatos. Essa descoberta levou à suposição de que se trata de um patógeno emergente que precisa ser monitorado, segundo o Goldenberger. Em 2022, os pesquisadores canadenses deram o nome à bactéria de Vandammella animalimorsus (mordida de animal Vandammella).
O próximo passo da equipe de Basileia é nomear suas novas espécies, e estão fazendo isso em colaboração estreita com o Dr. Peter Vandamme, professor da Universidade de Ghent (Bélgica) e especialista em classificação de bactérias. Até o momento, duas já receberam nomes: Pseudoclavibacter triregionum, referindo-se à localização de Basileia próxima às fronteiras da Suíça, França e Alemanha.
**Esta reportagem reflete exclusivamente a opinião do entrevistado.**