
Raiva humana no Brasil: ameaça silenciosa dos morcegos e saguis
Estudo publicado na RSBMT revela aumento de casos ligados a animais silvestres e expõe falhas no acesso à prevenção em comunidades vulneráveis
13/08/2025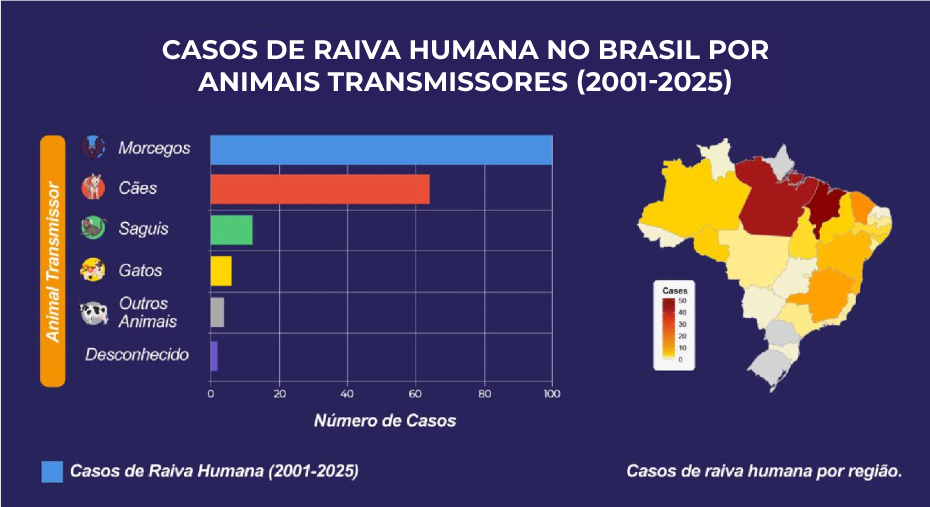
Em áreas remotas, como a Amazônia, o contato com morcegos eleva o risco de infecção pelo vírus da raiva, uma doença letal que desafia o sistema de saúde brasileiro
Um estudo publicado na Revista da Sociedade Brasileira de Medicina Tropical (RSBMT) apresenta uma análise abrangente dos casos de raiva humana no Brasil entre 2001 e 2025, revelando uma transição preocupante de uma zoonose tropical historicamente associada a cães domésticos para uma ameaça impulsionada por reservatórios silvestres, como morcegos e primatas. Intitulado “Two Decades of Human Rabies in Brazil: Epidemiological Trends, Emerging Risks, and Treatment Challenges“, o trabalho expõe desafios persistentes no controle dessa doença letal, que, embora prevenível, continua a vitimar populações vulneráveis por falhas no acesso à profilaxia, barreiras estruturais e mudanças ambientais.
A raiva, causada pelo vírus Lyssavirus rabies da família Rhabdoviridae, provoca encefalite aguda e progressiva, com taxa de letalidade próxima a 100% na ausência de tratamento adequado. A principal via de transmissão é a mordida ou o contato com saliva de animais infectados, embora casos por contato com mucosas também tenham sido relatados. O Brasil avançou significativamente no controle da raiva canina, com campanhas de vacinação em massa a partir de 2003, alinhando-se à meta da Organização Pan-Americana da Saúde (OPAS/OMS) de eliminar a transmissão canina até 2030. No entanto, segundo o estudo, os morcegos, particularmente o Desmodus rotundus (morcego hematófago), tornaram-se os principais vetores, responsáveis por 53,19% dos 188 casos de raiva humana registrados no período do estudo. “Mapear essas transformações epidemiológicas é essencial para formular respostas mais eficazes em territórios onde a prevenção ainda não chega com a força necessária”, afirma a médica veterinária Raquel Gomes Catozo, autora responsável pela idealização e liderança da pesquisa.
Entre 2001 e 2025, foram registrados 188 casos de raiva humana no Brasil, com média de 7,52 por ano. As regiões Norte e e Nordeste concentraram a maioria dos casos, com 68 e 95 registros, respectivamente. Pará e Maranhão lideram em número absoluto, com destaque para surtos nos anos de 2004, 2005, 2018 e 2022. As regiões Sudeste (18 casos), Centro-Oeste (6 casos) e Sul (1 caso) apresentaram menor incidência, enquanto Amapá, Rio Grande do Sul e Paraná não registraram nenhum caso. Dentre os transmissores, os morcegos predominaram com 100 ocorrências, seguidos por cães (64), primatas não humanos (12), gatos (6), outros animais (4) e fontes desconhecidas (2). O declínio dos casos caninos reflete o sucesso das campanhas de vacinação, que entre 2000 e 2009 alcançaram uma cobertura média de 86%, imunizando cerca de 21,4 milhões de animais por ano, 82% deles cães. Contudo, essa cobertura caiu para 60,4% em 2024, segundo dados do Ministério da Saúde, indicando fragilidade no atual sistema de prevenção. Para a pesquisadora, embora o Brasil tenha avançado no controle da raiva canina, falhou em acompanhar a dinâmica crescente da transmissão silvestre.
A emergência dos reservatórios silvestres representa um dos principais desafios. O Desmodus rotundus permanece como um vetor dominante, mas o aumento de casos atribuídos a primatas não humanos, especialmente os saguis (Callithrix jacchus e Callithrix penicillata), preocupa, sobretudo no Nordeste. Dez dos doze casos envolvendo primatas ocorreram no Nordeste, região onde a posse ilegal de saguis como animais de estimação é comum. Uma pesquisa publicada em 2011 identificou uma variante viral exclusiva desses primatas, sugerindo um possível ciclo de transmissão independente. Em 2025, dois casos confirmado no Ceará e em Pernambuco reforçaram a necessidade de vigilância em áreas urbanas, onde o contato com saguis é frequente. “A presença desses animais em áreas urbanas, muitas vezes mantidos como animais de estimação de forma ilegal, representa um risco real à saúde pública. Esses primatas, embora pareçam inofensivos, podem ser portadores de variantes pouco conhecidas e subnotificadas do vírus da raiva”, alerta a M.V. Catozo.
Casos de transmissão secundária também acendem o alerta. Entre 2015 e 2019, quatro pessoas contraíram raiva após contato com gatos infectados pela variante AgV3, originária de morcegos. Esses episódios ilustram como a interação entre animais silvestres e domésticos amplia o risco, sobretudo em locais onde a vacinação de felinos é negligenciada. A ausência de dados sistematizados sobre a imunização de gatos no Brasil é uma lacuna crítica. A variante AgV3 foi também identificada em morcegos frugívoros, como Artibeus lituratus, nos estados de Tocantins, Rondônia e Roraima, indicando que o vírus circula em diferentes espécies por coabitação de habitats.
As alterações ambientais, como desmatamento e mudanças climáticas, contribuem para o avanço da raiva silvestre. Em 2004, atividades de extração de madeira em Portel (Pará) foram associadas a surtos após a destruição de habitats forçar a aproximação de morcegos a áreas habitadas. Casos registrados em comunidades ribeirinhas da Amazônia (2018) e indígenas em Minas Gerais (2022) evidenciam a vulnerabilidade de populações que vivem longe de centros de saúde. Ribeirinhos, indígenas, trabalhadores rurais e ecoturistas estão entre os grupos mais expostos, devido à convivência próxima com animais silvestres e ao difícil acesso a serviços de prevenção. “São justamente esses grupos que mais sofrem com a falta de acesso à profilaxia e à informação sobre os riscos da raiva”, assinala a autora.
O estudo também analisa o perfil das vítimas. Homens foram maioria (107 dos 163 casos com dados disponíveis), possivelmente devido à maior exposição ocupacional. Crianças e adolescentes entre 10 e 14 anos (34 casos) e adultos entre 20 e 39 anos (42 casos) foram os mais afetados. A maioria dos registros envolveu mordidas ou arranhões (56 casos), mas 59 tiveram origem em contatos indiretos e 48 não informaram o tipo de exposição, evidenciando falhas nos registros epidemiológicos.
A profilaxia pós-exposição (PEP), composta por vacina antirrábica e, em casos graves, imunoglobulina (RIG), é a principal ferramenta para evitar o desenvolvimento da doença. Apesar de disponibilizada gratuitamente pelo Sistema Único de Saúde (SUS), a cobertura da PEP é insuficiente. Entre 2007 e 2021, apenas 17 dos 57 casos confirmados receberam PEP documentada. Em 27, não houve aplicação do protocolo, e em 12 não havia registros. A média de tempo entre a exposição e o início dos sintomas foi de 38,6 dias, enquanto o início da PEP ocorreu, em média, 30,6 dias após a exposição, frequentemente fora do tempo ideal. Em sete casos, a vacinação começou após o surgimento dos sintomas, contrariando as diretrizes da Organização Mundial da Saúde (OMS), que recomendam administração imediata. A doença avançou rapidamente: a média entre o início dos sintomas e o óbito foi de apenas 17dias. “A PEP salva vidas, mas precisa ser administrada imediatamente. O que vemos, infelizmente, são barreiras logísticas, desinformação e uma baixa percepção de risco tanto da população quanto dos próprios profissionais de saúde em áreas remotas”, afirma a médica veterinária.
Apenas dois pacientes sobreviveram à infecção. Ambos tratados com o Protocolo de Recife, uma adaptação brasileira do Protocolo de Milwaukee, desenvolvido nos Estados Unidos. O primeiro caso ocorreu em 2008, com um adolescente de 15 anos em Pernambuco que sobreviveu após receber PEP quatro dias após a exposição a morcego. O segundo foi registrado em 2017, com outro adolescente no Amazonas, que sobreviveu inicialmente, mas faleceu em 2025 em decorrência de sequelas neurológicas. O protocolo nacional prioriza o controle de eletrólitos, sedação profunda e antivirais, mas sua eficácia depende de intervenção precoce e cuidados intensivos. A hiponatremia, complicação frequente, exige controle rigoroso com dosagens diárias de sódio sérico.
As informações foram extraídas de bases como DataSUS, Sinan Net, Sistema de Informação do Programa Nacional de Imunização (PNI), PubMed, SciELO e Google Scholar. Contudo, inconsistências nos registros dificultam análises completas. Dos 188 casos, 25 não estão no Sinan, sendo mencionados apenas em relatórios do Ministério da Saúde. A falta de atualização do Sinan desde 2021 e a escassez de dados sobre vacinação felina comprometem o planejamento de ações. Antes de 2007, a escassez de registros clínicos confiáveis limitou a análise do manejo e da resposta profilática.
O estudo propõe soluções. A ampliação de campanhas de vacinação para incluir animais de criação e silvestres em áreas de risco é uma medida prioritária. Campanhas educativas voltadas à população sobre os riscos da raiva e a importância da profilaxia (PEP) são igualmente fundamentais. “A integração de inteligência artificial para análises preditivas, já testada em países como Marrocos e Haiti, é sugerida como uma ferramenta promissora para otimizar a vigilância no Brasil, embora ainda não tenha sido adotada localmente. Pesquisas in silico para o desenvolvimento de antivirais, como aquelas que avançaram tratamentos para HIV e SARS-CoV-2, são sugeridas como uma abordagem viável para acelerar terapias contra a raiva, reduzindo custos e tempo”, acrescenta a M.V. Catozo.
A meta da OPAS/OMS de eliminar as mortes por raiva canina até 2030 exige o fortalecimento da vigilância, o acesso universal à PEP e a capacitação permanente de profissionais. A baixa percepção de risco, sintomas inespecíficos, falhas no atendimento inicial e a escassez de treinamento, como constatado em um estudo de 2014 no Maranhão, onde 39,3% dos profissionais nunca haviam recebido capacitação sobre raiva, continuam a comprometer o enfrentamento da doença.
Globalmente, a raiva causa cerca de 55 mil mortes anuais, principalmente na Ásia e na África, onde a transmissão canina é predominante. No Brasil, o controle da raiva canina é um sucesso relativo, mas a transmissão silvestre permanece como obstáculo crescente. Desde a vacina de Pasteur, em 1885, até os protocolos modernos, a história da raiva reflete avanços e desafios. Ainda classificada como doença negligenciada, afeta desproporcionalmente comunidades vulneráveis, como populações rurais, ribeirinhas e indígenas, nas quais a pobreza e o isolamento geográfico amplificam o risco. “Estamos falando de uma doença 100% evitável, mas que continua matando porque permanece invisível para a maioria das políticas públicas. A raiva é silenciosa, letal e ainda muito negligenciada”, encerra a M.V. Catozo.
Confira o artigo “Two Decades of Human Rabies in Brazil: Epidemiological Trends, Emerging Risks, and Treatment Challenges” publicado na Revista da Sociedade Brasileira de Medicina Tropical (RSBMT): https://doi.org/10.1590/0037-8682-0110-2025.
**Esta reportagem reflete exclusivamente a opinião do entrevistado.**








